近日,国药集团已提交新冠疫苗上市申请的消息引发了大家的关注,国药集团新冠疫苗将成为国内首批上市的新冠疫苗,从国内目前的疫情来看国产新冠疫苗的进度是全国人民关注的首要话题,毕竟新冠病毒的传播能力十分强,接种新冠疫苗能让大家更有效的避免感染病毒,那么下面大家和微闻网小编一起去了解一下国药集团已提交新冠疫苗上市申请,新冠疫苗国产的好还是进口的好~

国药集团已提交新冠疫苗上市申请
据报道,国药集团有限公司副总经理石晟怡表示,国药集团已向国家药监局提交了新冠疫苗上市申请。
国药集团有两款灭活新冠疫苗,由旗下中国生物研发,国药集团持股占比95%,但中国生物本身并非上市公司。
受此利好消息影响,国药系其他上市公司股价直线拉升,其中国药股份(600511.SH)一度大涨近9%,国药一致(000028.SZ)涨近4%,国药控股(01099.HK)涨近4%,天坛生物(600161.SH)上涨2.29%,现代制药上涨1.64%。
公开资料显示,国药集团是由国务院国资委直接管理的唯一一家以医药健康产业为主业的中央医药企业,旗下有1500余家子公司和国药控股、国药股份、国药一致、天坛生物、现代制药、中国中药6家上市公司。
11月18日,国药集团官方发布川观新闻对国药集团党委书记、董事长刘敬桢的采访,在采访中,刘敬桢提到,在新冠疫苗的紧急使用方面,国药集团现在已经在近百万人上进行使用,没有接到一例严重不良反应的报告,只有个别的有一些轻微症状。
此前的进博会期间,刘敬桢曾在第三届虹桥国际健康科技创新论坛上表示,目前为止,数十万人紧急接种了国药集团旗下的新冠疫苗,没有一例严重不良反应,其中注射疫苗后的离境人员,有5.6万人,目前无一例感染。
假设企业提交了新冠疫苗上市申请,距离其被审批通过和民众可以大范围使用还有多少程序和步骤,以及时间?
7月22日,我国正式启动新冠疫苗紧急使用。根据《疫苗管理法》明确规定,当出现特别重大公共卫生事件,由国家卫生健康委提出紧急使用疫苗的申请,由国家药监局组织专家论证并同意,由国家卫生健康委在一定范围、一定时限内紧急使用疫苗。
对于新冠疫苗的审评审批,早在3月30日,国家市场监管总局就公布《药品注册管理办法》和《药品生产监督管理办法》,明确疾病预防、控制急需的疫苗和创新疫苗可申请适用优先审评审批程序。
在《药品上市许可优先审评审批工作程序》(下称《工作程序》)规定,对于符合“临床急需的短缺药品、防治重大传染病和罕见病等疾”等药品可以走优先审评审批工作程序。
《工作程序》规定:
1、申报前沟通交流。申请人在提出药品上市许可申请前,应当与国家药品监督管理局药品审评中心(下称“药审中心”)进行沟通交流,探讨现有研究数据是否满足药品上市许可审查要求以及是否符合优先审评审批程序纳入条件等,对于初步评估认为符合优先审评审批纳入条件的,应当在会议纪要中予以明确。
2、申报与提出申请。经沟通交流确认后,申请人应当在提出药品上市许可申请的同时,通过药审中心网站提出优先审评审批申请,并提交相关支持性资料。申请人在药审中心网站提交的相关支持性资料应当与申报资料内容一致。
3、审核。药审中心应当在接到申请后 5 日内对提交的优 先审评审批申请进行审核,并将审核结果反馈申请人。拟纳入优 先审评审批程序的,应当按要求在药审中心网站对外公示。
4、公示纳入。药审中心对拟纳入优先审评审批程序的品种具体信息和理由予以公示,包括药物名称、申请人、拟定适应症(或功能主治)、申请日期、拟纳入理由等。
5、技术审评。药审中心对纳入优先审评审批程序的药品 上市许可申请,按注册申请受理时间顺序优先配置资源进行审 评。对纳入优先审评审批程序的药品上市许可申请,审评时限为 130 日,其中临床急需的境外已上市境内未上市的罕见病药品审 评时限为70 日。
6、核查、检验和通用名称核准。对纳入优先审评审批程 序的药品上市许可申请,需要进行核查、检验和核准通用名称的, 药品核查中心、药品检验机构和国家药典委员会应优先进行核 查、检验和核准通用名称。7. 经沟通交流确认,补充提交技术资料。8. 综合审评。9、审批。
除此之外,在发生突发公共卫生事件的威胁时,以及突发公共卫生事件发生后,还有一个“快速通道”——“特别审批程序”,是指国家药监局可以依法决定对突发公共卫生事件应急所需防治药品实行特别审批,对实施特别审批的药品注册申请,国家药监局将加快并同步开展药品注册受理、审评、核查、检验工作。特别审批的情形、程序、时限、要求等按照《药品特别审批程序》的规定执行。
随着国药集团已提交新冠疫苗上市申请的消息传出,以及辉瑞等进口疫苗的也即将上市的情况来看,人们开始普遍关心起国产的新冠疫苗和进口疫苗到底有什么区别,哪个更为先进可靠的话题。其实关于这个问题,此前不就钟南山就曾经表态。
钟南山表示,目前,新冠还有很多主要问题没有解决,新冠疫情发生的规律还没有摸清,溯源尚未完成,也没有极具针对性且非常有效的药物。国外辉瑞疫苗能阻止90%的感染,中国的疫苗研发也在差不多水平,但要有了第一阶段试验结果才能公布。
随着美国疫苗及英国疫苗相继公布确切有效率,市场也开始关注中国疫苗何时公布有关疫苗的有效性数据,毕竟根据世卫组织的统计,中国已有4款新冠疫苗进入了三期临床试验,在全球疫苗研发中走在前列。如今国药集团已提交新冠疫苗上市申请,更进一步。
除了国药集团已提交新冠疫苗上市申请之外,中国已进入三期临床试验的疫苗,在2021年将达到19亿剂的产量,满足本国需求的同时,还可向别国提供。
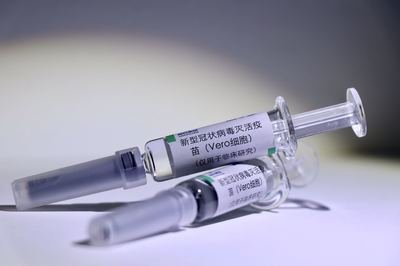
新冠疫苗市场几家欢乐几家愁
当地时间11月22日,美国政府疫苗研发项目“曲速行动”负责人Moncef Slaoui对CNN表示,美国首批新冠肺炎疫苗接种“很有希望”在三周内启动。
当地时间11月20日,美国制药公司辉瑞表示,已经向美国食品药品监督管理局递交了关于新冠疫苗的紧急使用授权,如申请通过,美国最早将于12月开始限量投放疫苗。新冠疫苗的基准价格为每剂19.5美元,不过此价格仅限于美国。
该公司上旬宣称其新冠疫苗试验取得了积极成果,其候选疫苗的有效性超过90%,远超了美国食药品管理局(FDA)想要的和投资者的预期。彼时消息一出,投资者的狂热情绪一触即发,大盘开盘后大幅走高,当天早些时候涨幅逼近5%。
11月23日消息,Moderna首席执行官介绍,政府正在寻求订购Moderna的潜在新冠疫苗,每剂量的价格或在25美元至37美元之间,具体取决于订购的数量。
Moderna预计,到2020年底,将准备在美国运送约2000万剂新冠疫苗,并有望在2021年在全球生产5亿-10亿剂。
与此同时,最早参与疫苗研发的阿斯利康公司也发布消息,公司新冠疫苗有效率可达90%,而且比辉瑞和Moderna疫苗便宜许多。
争先恐后的不只是辉瑞、Moderna和阿斯利康,根据伦敦卫生与热带医学学院疫苗中心追踪器的数据,与上述三家公司的疫苗一样,处于三期试验阶段的还有另外8款疫苗。
强生公司首席科学家称,2021年之前新冠肺炎试验将招募6万人参与,预计能在明年1-2月知道新冠疫苗的效用。
葛兰素史克(GSK)北京时间11月23日宣布,评估其呼吸道合胞病毒(RSV)候选疫苗用于母体免疫(GSK3888550A疫苗)安全性和有效性的3期GRACE研究(NCT04605159)已开始对受试者进行疫苗接种。该研究预计2024年初结束,中期结果预计2022年下半年公布。
同日,备受全世界瞩目,且其“抗体鸡尾酒疗法”得以让特朗普的痊愈再生元制药Regeneron Pharmaceuticals, Inc.(代码REGN)也宣布其新冠抗体治疗药物将很快得到更广泛的应用,公司将于明年1月向美国提供30万剂新获授权的新冠抗体治疗药物。
REGN指出,其公司每月能生产10万剂。与此同时,该公司正在测试是否可以将所需剂量减半。如果可以的话,这将是现有治疗方法的两倍。
这是对抗新冠病毒的又一个积极的势头。虽然抗体治疗不是一种治疗方法,但它们在疫苗上市前的争取时间方面发挥着关键作用。让在接下来的几个月里,治疗呼吸系统疾病的医院和医疗机构可以有更充分的准备。
几家欢乐几家愁,当FDA对生物技术公司Inovio Pharmaceuticals 计划进行的第2/3期试验进行新冠肺炎疫苗试验部分临床试验搁置时,该公司股价下降了28%,而年前至夏天Inovio涨幅接近10倍。
特别声明:以上内容来源于编辑整理发布,如有不妥之处,请与我方联系删除处理。邮箱:taopano06999@163.com









