11月18日,美国辉瑞和德国生物科技公司BioNTech发布了有关新冠疫苗的最新消息,消息中辉瑞称其疫苗有效率达95%,并且将会在近日提交紧急授权的申请,辉瑞疫苗或成为首家美国官方批准疫苗,同时辉瑞白表示辉瑞新冠疫苗或在“圣诞前”开始交付,也就是说美国人民很快就能用到新冠疫苗了,那么美国辉瑞新冠疫苗最新消息怎么样了呢?让我们一起去了解一下吧~
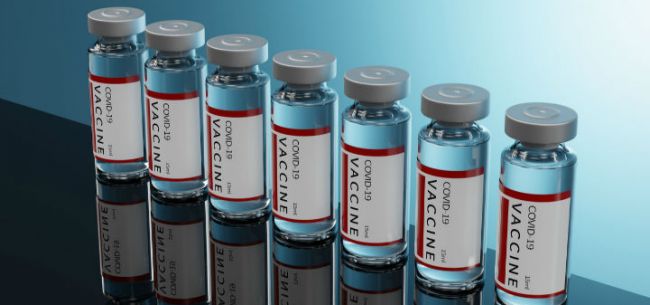
辉瑞称其疫苗有效率达95%
美国辉瑞和德国生物科技公司BioNTech于当地时间18日表示,其共同开发的新冠疫苗有效率已经由上周宣布的90%提高到95%,将于近日提交紧急使用授权的申请。
据美国全国广播公司(NBC)18日报道,辉瑞公司在一份联合声明中表示,其与BioNTech共同开发的新冠疫苗有效率已经由上周宣布的90%提高到95%,在接受疫苗试剂的41135名成年人均没有出现严重的副作用,3.7%的受试者感到疲劳,2%的受试者感到头痛,但这都属于正常反应。
辉瑞董事长兼首席执行官阿尔伯特·布尔拉在声明中写道:“这项研究结果显示(我们)在研制疫苗的历史性征途中迈出了重要的一步。”他表示,“全球每天都有数十万人感染,我们迫切需要向全世界提供一种安全有效的疫苗。”
声明指出,辉瑞将在“几天内”向美国食品药品监督管理局(FDA)提交紧急使用授权申请,同时与欧洲和其他地区的监管机构分享他们的数据。
据此前报道,这两家公司曾于上周表示,在首批感染新冠病毒并出现至少一种症状的94名受试者中,疫苗的有效性被证明超过90%。
据悉,FDA在今年10月就新冠疫苗作紧急使用授权标准发布了一份指导意见,要求在授权紧急使用任何实验性新冠疫苗之前,制造商必须掌握至少两个月的安全数据。该审批标准的提高旨在提高透明度和公众信任度,保证不会因为政治干预而匆忙对安全性和有效性没有得到充分保障的新冠疫苗作授权。
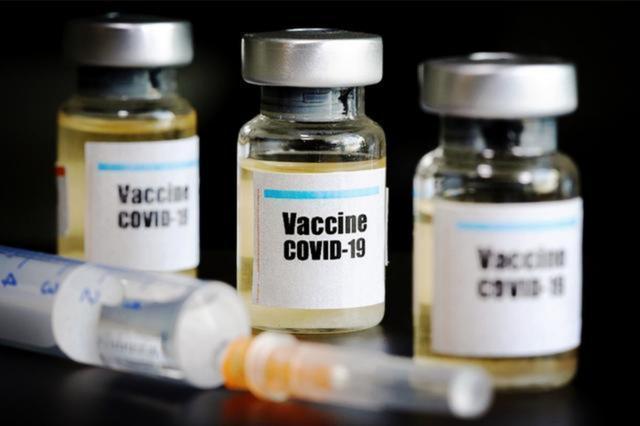
辉瑞疫苗或成为首家美国官方批准疫苗
综合美国ABC新闻报道,当地时间18日,辉瑞公司(Pfizer)及其合作伙伴生物科技公司(BioNTech)宣布,经过大规模三期试验的最终分析,他们的新冠病毒疫苗有效性超过95%,已经达到了一个关键的安全性里程碑,这将使公司能够“在几天内”紧急申请美国食品药品管理局(FDA)的批准。
如果FDA给该疫苗开绿灯,辉瑞可能会成为第一家获得FDA批准的新冠疫苗公司。该公司表示,一旦政府疫苗获得批准,可能在2020年底之前,该公司一夜之间就能向易感人群提供数百万剂的新冠“救命”疫苗。
就在上周,辉瑞和生物科技宣布,根据对首批94名出现症状的新冠患者的初步分析,他们的新冠疫苗的有效性超过了90%。
在其发布的一份新闻稿中,辉瑞宣布,在170名参与新冠临床试验的志愿者中,他们的疫苗使162人被治愈。
这意味着辉瑞公司的疫苗在预防新冠症状方面的有效性约为95%。另外,其竞争对手Moderna宣布,他们的疫苗的初步分析有效性为94.5%。
目前还不清楚接种疫苗后的免疫程度以及免疫持续时间。试验志愿者将被跟踪两年,以检测诸如疫苗的持久性等问题。
辉瑞公司周三还宣布了另一个重要数据:FDA要求至少一半的试验志愿者提供两个月以上的安全数据,然后才会考虑授予有限的紧急授权。辉瑞现在已经达到了该标准,公司申请这一授权可能就在未来几天。
一旦FDA收到辉瑞的申请,它将审查数据,并召集外部专家小组就是否批准疫苗提出意见。然后,FDA将做出最终决定。
据悉,即使辉瑞的疫苗获得批准,该公司也可能面临物流障碍。与Moderna生产的类似疫苗不同,辉瑞的疫苗必须储存在华氏零下94度的超低温下。
辉瑞已承诺通过正式的科学审查程序、公布试验的全部细节。有关试验的其他细节将通过FDA的审查程序公布,并承诺信息将对公众透明。
周三的新闻稿包含了有关疫苗有效性的一些新细节,包括它似乎对所有种族群体都同样有效。与此同时,该疫苗对65岁以上成年人的有效性“超过94%”。
辉瑞在其临床试验中没有出现过任何严重的安全问题。像大多数疫苗一样,辉瑞的疫苗——三周内注射两次——会产生轻微的副作用。最常见的“3级”副作用是疲劳,约有3.7%的志愿者出现这种情况,2%的志愿者出现头痛状况。
辉瑞和生物科技还表示,它们也在计划请求欧洲药品管理局(European Medicines Agency,欧洲版的FDA)允许它们在欧洲销售这种疫苗。
根据新闻稿,这两项申请可能会在“几天内”发布。辉瑞公司说,到今年年底,他们可以生产5000万剂疫苗,这足够为2500万人提供疫苗,因为每个人需要注射两次。
到2021年,辉瑞预计将能在全球生产13亿剂新冠疫苗。
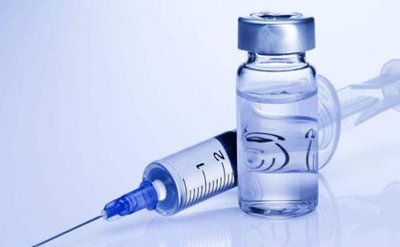
辉瑞/BioNTech新冠疫苗或在“圣诞前”开始交付
路透社11月18日消息,辉瑞和BioNTech周三表示,他们的新冠疫苗可能将于下月获得美国和欧洲的紧急授权,此前公布的最终试验结果显示,该疫苗有效性高达95%,且没有严重副作用。
研究发现,这种疫苗的效力在不同年龄和种族之间是一致的——考虑到这种病毒对老年人和包括黑人在内的某些群体造成了不成比例的伤害,这是一个有希望的迹象。
BioNTech首席执行官Ugur Sahin对路透电视表示,美国食品药品监督管理局(FDA)可能在12月中旬批准紧急使用。他补充称,12月下半月可能会获得欧盟有条件的批准。他说,“如果一切顺利,我可以想象我们会在12月下半月获得批准,并在圣诞节前开始交付,但前提是一切顺利。”
Sahin说,周五将申请美国紧急使用授权(EUA)。据知情人士透露,FDA顾问委员会暂定于12月8-10日开会讨论疫苗,不过日期可能会改变。FDA没有回应置评请求。
美国新冠肺炎确诊病例累计超1116万例
美国约翰斯.霍普金斯大学发布的新冠疫情最新统计数据显示,截至美东时间11月16日16时27分,美国新冠肺炎累计确诊病例超过1116万例,为11163990例,死亡病例为246953例。较前一日同一时间相比,在过去24小时内,美国新增确诊病例163006例,新增死亡病例947例。
特别声明:以上内容来源于编辑整理发布,如有不妥之处,请与我方联系删除处理。邮箱:taopano06999@163.com









